Натрий гидроокись, что это. Гидроксид натрия — распространенная и полезная щелочь
- Натрий гидроокись, что это. Гидроксид натрия — распространенная и полезная щелочь
- Натрий гидроокись ЧДА, что это. Натрия гидроокись ЧДА
- Натрий хлористый. Натрия хлори. 9% - Биеффе медитал - инструкция по применению
- Натрий гидроокись, что это такое. Что такое гидроксид натрия
- Натрий сернокислый. Химические свойства
- Видео натрий гидроокись или же просто - едкий натр.
Натрий гидроокись, что это. Гидроксид натрия — распространенная и полезная щелочь
- — Как и другие щелочи, этот химикат является сильным основанием, которые, как известно, отлично растворяются в воде, что сопровождается сильным выделением тепла.
- — Гидроокись натрия может буквально растворяться, находясь на воздухе, так как невероятно гигроскопична и вбирает влагу из окружающей среды. Это значит, что хранить ее необходимо в плотно укупоренной таре и в сухом помещении. Иногда ее хранят в виде раствора в воде, этиле или метаноле.
- — Горячий раствор или расплавленный реактив нежелательно помещать в емкости из стекла или фарфора — это может повредить их, поскольку каустик вступает в реакцию с кремнеземом в их составе. Лучше для гидроксида натрия купить емкость из полиэтилена, поливинилхлорида или резины.
- — Мыловарение, производство бумаги и картона, косметики, растворителей, биодизельного топлива и минеральных масел.
- — Обработка древесины, нейтрализация ядовитых газов и кислот.
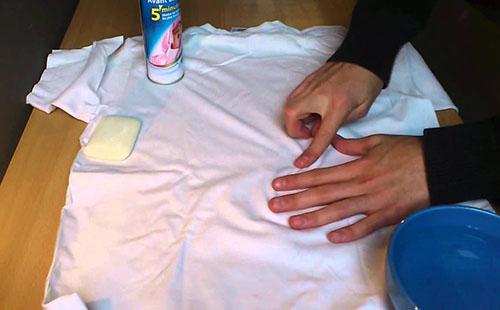
- — В медицине: удаление ороговевшей кожи и папиллом, лечение бородавок.
- — В качестве чистящего и дезинфицирующего средства, в химической промышленности в качестве катализатора.
- — В пищевой промышленности, в частности для придания темного окраса и мягкости оливкам, для получения хрустящей корочки на выпечке, при изготовлении какао.
Данный реактив, самая распространенная щелочь, более известен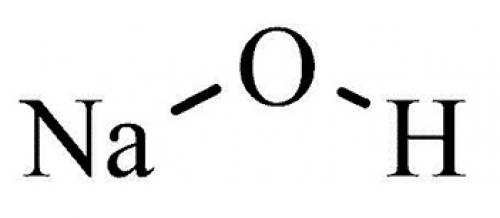 под названиями едкий натр или каустическая сода (от французского слова sodium — натрий и греческого слова kaustikos — едкий). Исходя из названия понятно, что вещество опасное, поэтому обращаться с ним надо бережно. Гидроокись натрия — бесцветная кристаллическая масса. Вещество способно разъедать не только материалы органического происхождения, но и определенные металлы, причем при контакте с цинком, свинцом, алюминием, оловом и их сплавами выделяется водород, взрывоопасный газ. Нельзя допускать контакта каустической соды с аммиаком, это пожароопасно.
под названиями едкий натр или каустическая сода (от французского слова sodium — натрий и греческого слова kaustikos — едкий). Исходя из названия понятно, что вещество опасное, поэтому обращаться с ним надо бережно. Гидроокись натрия — бесцветная кристаллическая масса. Вещество способно разъедать не только материалы органического происхождения, но и определенные металлы, причем при контакте с цинком, свинцом, алюминием, оловом и их сплавами выделяется водород, взрывоопасный газ. Нельзя допускать контакта каустической соды с аммиаком, это пожароопасно.
Важные особенности гидроксида натрия
Их важно знать, чтобы работа с этим реактивом была безопасной, и чтобы его применение принесло ожидаемые результаты.
Основные сферы применения едкого натра

Техника безопасности в работе с гидроксидом натрия
По ГОСТ 12.1.007-76 каустическая сода относится ко II классу токсичности (высокоопасна). Может вызвать сильный ожог кожи и слизистых, необратимое повреждение зрения при попадании в глаза. Именно поэтому работать с ней нужно в перчатках и защитных очках , использовать специальную одежду с виниловой пропиткой или прорезиненную.
При попадании вещества на слизистую ее как можно скорее нужно промыть большим количеством проточной воды, кожу промыть слабым раствором уксуса.
При большой поверхности ожога, при попадании реактива внутрь или в глаз следует не только приянть эти меры, но и незамедлительно обратиться к врачу.
Вы можете купить щелочь гидроксид натрия в нашем магазине, и мы надеемся, что вы будете соблюдать технику безопасности. Товар продается с доставкой, поэтому вы можете купить щелочь в Москве или другом городе России и вскоре получить его в своем городе.
Натрий гидроокись ЧДА, что это. Натрия гидроокись ЧДА
Синонимы:
Гидроксид натрия ЧДАФормула:
NaOHСтандарт:
 Описание:
Описание:
Натрия гидроокись ЧДА - чешуированная масса белого цвета, сильно гигроскопичная, хорошо растворимая в воде и спирте, быстро поглощает из воздуха углекислоту и воду.
Применение:
Натрия гидроокись ЧДА применяется в производстве химических волокон, ионообменных смол, химических реактивов, в целлюлозно-бумажной, медицинской промышленности, черной и цветной металлургии и других отраслях народного хозяйства.
Натрия гидроокись ЧДА ГОСТ 4328-77
| Массовая доля гидроксида натрия, %, не менее | 98 |
| Массовая доля углекислого натрия, %, не более | 1,0 |
| Массовая доля общего азота, %, не более | 0,0005 |
| Массовая доля кремнекислоты, %, не более | 0,002 |
| Массовая доля сульфатов (SO4), %, не более | 0,0050 |
| Массовая доля хлоридов, %, не более | 0,0050 |
| Массовая доля фосфатов, %, не более | 0,0030 |
| Массовая доля алюминия, %, не более | 0,0010 |
| Массовая доля железа, %, не более | 0,0010 |
| Массовая доля кальция и магния, %, не более | 0,024 |
| Массовая доля калия, %, не более | Не нормируется |
| Массовая доля тяжелых металлов, %, не более | 0,00100 |
| Массовая доля мышьяка, %, не более | Не нормируется |
Упаковка:
- Гидроокись натрия ЧДА упаковывают
- в потребительскую тару:- стеклянные банки с навинчивающейся крышкой из полимерного материала (или алюминия), имеющую полиэтиленовый вкладыш;- полиэтиленовые или пропиленовые банки с навинчивающейся крышкой и вкладышем или прокладкой из того же материала;- пакеты из неокрашенной полиэтиленовой пленки
- транспортную тару: мешки из неокрашенной полиэтиленовой пленки; металлические барабаны по 80 кг с мешками-вкладышами из полиэтиленовой пленки др.
Хранение:
Гидроокись натрия ЧДА хранят в упаковке изготовителя в закрытых складских помещениях. Гарантийный срок хранения продукта – 6 месяцев со дня изготовления.
Транспортировка:
Гидроокись натрия ЧДА перевозят всеми видами транспорта в соответствии с правилами перевозок грузов, действующими на данном виде транспорта.
Техника безопасности:
Гидроокись натрия пожаро- и взрывобезопасна, по степени воздействия на организм относится к веществам 2-го класса опасности.
Натрия гидроокись ЧДА реализует компания "Логосиб".
Цены:
Несмотря на изначально низкие цены, мы делаем скидки в зависимости от объема закупаемого товара.
Качество:
Мы работаем непосредственно с производителями, поэтому обеспечиваем наших клиентов товарами высокого качества.
Оформление и отгрузка:
Благодаря отлаженной работе офиса и складов, мы предоставляем быстрое оформление и отгрузку товаров.
Доставка:
Мы предлагаем доставку товаров по России:•автотранспортом;•железнодорожными контейнерами, вагонами;•через транспортные компании.
Натрий хлористый. Натрия хлори. 9% - Биеффе медитал - инструкция по применению
Официальная инструкция, зарегистрированная Минздравом РФ (по grls.rosminzdrav.ru)
См. откуда получены инструкции МЕДИ РУ
ИНСТРУКЦИЯ
по медицинскому применению лекарственного препарата
Натрия хлорид
Торговое наименование препарата
Натрия хлорид
Международное непатентованное наименование
Натрия хлорид
Лекарственная форма
раствор для инфузий
Состав
В 1 л препарата содержится активное вещество: натрия хлорид 9 г.
Вспомогательное eeufecmeo: вода для инъекций до 1 л.
Описание
Прозрачный бесцветный раствор.
Фармакотерапевтическая группа
Регидратирующее средство
Код АТХ
B05CB01
Фармакодинамика:
Оказывает дезинтоксикационное и регидратирующее действие. Восполняет дефицит натрия при различных патологических состояниях организма и временно увеличивает объем жидкости циркулирующей в сосудах.
Фармакодинамические свойства раствора обусловлены наличием ионов натрия и хлорид-ионов. Ряд ионов в том числе ионы натрия проникают через клеточную мембрану при помощи различных механизмов транспорта среди которых большое значение имеет натрий-калиевый насос (Na-K-АТФаза). Натрий играет важную роль в передаче сигналов в нейронах электрофизиологических процессах сердца а также в метаболических процессах в почках.
Фармакокинетика:
Натрий выделяется преимущественно почками однако при этом большое количество натрия подвергается реабсорбции (почечная реабсорбция). Небольшое количество натрия выделяется с калом и при потоотделении.
Показания:
- Изотоническая внеклеточная дегидратация;
- Гипонатриемия;
- Разведение и растворение вводимых парентерально лекарственных веществ (в качестве базового раствора).
Противопоказания:
Гипернатриемия ацидоз гиперхлоремия гипокалиемия внеклеточная гипергидратация; циркуляторные нарушения угрожающие отёком мозга и лёгких; отёк мозга отёк лёгких острая левожелудочковая недостаточность сопутствующее назначение глюкокортикостероидов в больших дозах.
При добавлении в раствор других препаратов необходимо учитывать противопоказания к этим препаратам.
С осторожностью:
Декомпенсированнная хроническая сердечная недостаточность артериальная гипертензия периферические отёки преэклампсия хроническая почечная недостаточность (олиго- анурия) альдостеронизм и другие состояния связанные с задержкой натрия в организме.
Беременность и лактация:
Раствор можно вводить во время беременности и лактации.Способ применения и дозы:
Внутривенно (обычно капельно). Необходимая доза может рассчитываться в мЭкв или ммоль натрия массе ионов натрия или массе хлорида натрия (1 г NaCl = 394 мг 171 мЭкв или 171 ммоль Na и С1).
Доза определяется в зависимости от состояния пациента потери организмом жидкости Na+ и С1- возраста массы тела пациента. Следует тщательно контролировать сывороточные концентрации электролитов в плазме и моче.
Доза раствора натрия хлорида для взрослых составляет: от 500 мл до 3 л в сутки.
Доза раствора натрия хлорида для детей составляет: от 20 мл до 100 мл в сутки на кг массы тела (в зависимости от возраста и общей массы тела).
Скорость введения зависит от состояния пациента.
Натрий гидроокись, что это такое. Что такое гидроксид натрия
Это соединение – едкая щелочь, которая применяется не только пищевой, фармацевтической и косметической сферами, но и химической промышленностью. Гидроокись натрия, или каустическая сода, выпускается в виде немного скользких твердых гранул желтоватого или белого цвета. При сильной концентрации NaOH разъедает органические соединения, поэтому способен вызвать ожог. Используется как пищевая добавка Е524, необходимая для поддержания консистенции продуктов.
Формула
Вещество имеет химическую формулу NaOH. Соединение взаимодействует с различными веществами любых агрегатных состояний, нейтрализуя их, с кислотами, образуя соль и воду. Реакция с атмосферными оксидами и гидроксидами позволяет получить тетрагидроксоцинкат или алкоголят. Едкий натр применяется для осаждения металлов. Например, при реакции с сульфатом алюминия образуется его гидроксид. Осадок не растворяется и не наблюдается избыточное получение щелочи. Это актуально при очистке воды от мелких взвесей.
Свойства
Соединение растворяется в воде. Технический Sodium Hydroxide представляет собой водный раствор гидроксида натрия в щелочеустойчивой герметичной таре. При взаимодействии с водой каустик выделяет большое количество тепла. Вещество имеет следующие свойства:
- при предварительном расплавлении разрушает стекло, фарфор;
- взаимодействие с аммиаком вызывает пожароопасную ситуацию;
- кипит при 1390°С, плавится, если температура достигает 318°С;
- не растворяется в эфирах, ацетоне;
- очень гигроскопичен (поглощает пары воды из воздуха), поэтому натриевая щелочь должна храниться в сухом месте и герметичной упаковке;
- растворяется в метаноле, глицерине, этаноле;
- бурно взаимодействует с металлами – оловом, гидроксидом алюминия, свинцом, цинком, образует водород – взрывоопасный горючий яд;
- поглощает углекислый газ из воздуха.
минерала брусита . Второе по величине месторождение сконцентрировано на территории России. Гидроокись благодаря исследованиям Николы Леблана, проведенным в 1787 г., получают методом синтеза из хлористого натрия. Позже востребованным способом добычи стал электролиз. С 1882 г. ученые разработали ферритный метод получения в лаборатории гидроксида с помощью кальцинированной соды. Электрохимический способ сейчас самый популярный: ионы натрия образуют его раствор едкой ртути – амальгаму, которая растворяется водой.
Натрий сернокислый. Химические свойства
Сульфат Натрия, что это? Данное химическое соединение – это натриевая соль серной кислоты. Формула Сульфат Натрия: Na2SO4 . Это бесцветные кристаллы, устойчивые в безводной форме при температуре от 33 градусов Цельсия. При температуре ниже средство образует кристаллогидраты , формула Na2SO4•10H2O . Соленый на вкус кристаллический порошок имеет молярную массу 142 грамма на моль. В естественной среде вещество содержится в минерале тенардит, кристаллогидрат образует соединение мирабилит ( глауберова соль ). Вещество можно обнаружить в различных формах в рапе, на дне соленых озер.
Химические свойства. Что такое Сульфат Натрия? Формула Сульфат Натрия: Na2SO4 . Соединение проявляет свойства средней соли, так как образовано сильной серной к-ой и гидроксидом натрия (слабое основание). Вещество не подвергается гидролизу , так как не имеет в составе «слабого иона». Смесь гидросульфата и Сульфата Натрия может вступить в реакцию с раствором гидроксида натрия .
При электролизе раствора (водного) Натрия Сульфата на катоде выделяется водород, а на аноде кислород (из воды), в результате в катодном пространстве происходит обогащение ионами натрия, в анодном – ионами SO42- и водорода.
Качественная реакция на Сульфат Натрия проводится по аналогии с качественной реакцией на сульфат-ионы. К соли серной кислоты добавляют р-р хлорида бария , в результате чего образуется белый кристаллический осадок сульфата бария и соляная кислота . Отличить сульфат- от сульфит -иона можно с помощью азотной кислоты (раствор), полученный осадок при ее добавлении не растворится.
Вещество можно получить в промышленных масштабах при взаимодействии хлорида натрия с серной кислотой в специализированных печах, при высокой температуре от 500 до 550 градусов, побочных продуктом реакции является хлороводород . Но в связи с наличием больших запасов природного сырья, этот метод не применяют.
Сульфат Натрия можно использовать на производстве синтетических чистящих и моющих средств; при производстве стекла и целлюлозы; средство используют в текстильной промышленности, цветной металлургии, в кожевельной промышленности. Применяется в виде обезвоживающего средства в хим. лабораториях, в связи с тем, что оно дешево стоит и легко отфильтровывается. В медицине лекарство используют в качестве солевого слабительного и добавляют в состав растворов для промывания носа. Средство используют в виде пищевой добавки под кодом E514 .
 Описание:
Описание: